破骨細胞
破骨細胞は、骨芽細胞のような間葉系幹細胞ではなく、血球系の幹細胞である造血幹細胞からM-CSF(macrophage-colony simulating factor)らの作用により破骨細胞前駆細胞へと分化したあと、M-CSF-c-fms及び、RANKL-RANK(receptor activator of NF-κB ligand)刺激、免疫受容体を介した共刺により、多核化、つまり前駆破骨細胞同士の融合が起こって成熟破骨細胞へと分化する。
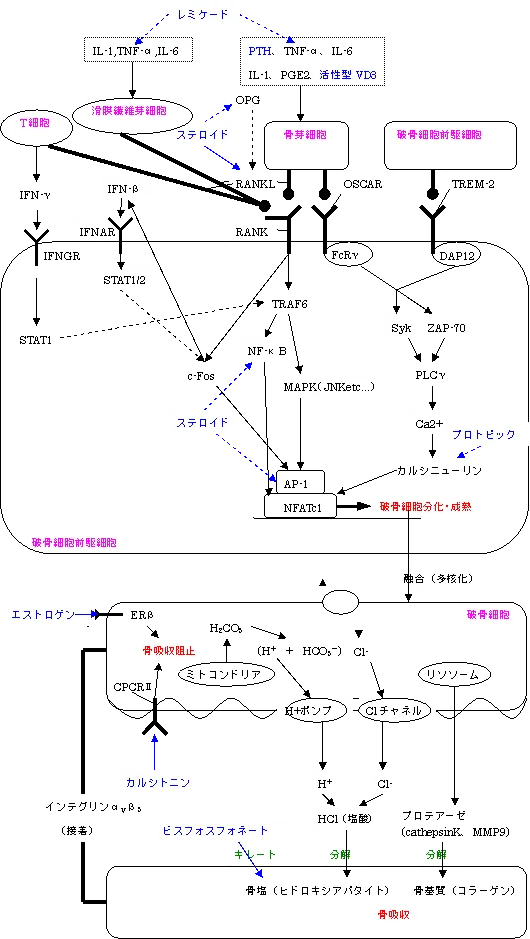
RANKL-RANK刺激は、TRAF6(TNF receptor associated factor 6)を介してNF-κB、MAPKを活性化する。
MAPK経路にて誘導されるAP-1はご存知の通りNFATc1に結合して転写活性を調節するが、NF-κBにより誘導されるNFATc1(nuclear factor of activated Tcell c1)は、プロトピックの機序と同じくその刺激だけでは核内へと移行できない。
核内への移行を進行させるためには、免疫受容体OSCAR、PIR-A、TREM-2及びSIRPβ1などがそれぞれに対応するFcRγ、DAP12といったITAMを持つアダプター分子と会合することで別経路が進行させる必要があり、これにより、Ca2+の活性化とNFATの脱リン酸化が起こって核内へと移行することができるようになる。
核内へと移行したNFATc1は、PU.1、MITFなどによっても活性化されて、TRAP(酒石酸耐性酸ホスファターゼ)、カテプシンK、カルシトニン受容体などの、破骨細胞特異的遺伝子の発現を誘導する。
一方、このような破骨細胞活性化シグナルに対して抑制化シグナルもいくつか存在している。その中でも重要なものとして、IFN-βと炎症時にT細胞 から産生されるIFNγ、RANKLを抑制するOPG(Osteoprotegerin)があり、IFN-βはSTAT1、2を介してc-fosを、IFN-γはSTAT1を介してTRAF6を抑制する。
こうして、多核破骨細胞へと分化した後は、ポドソームに集積したインテグリンαVβ3により接着し、塩酸分泌による石灰分の分解とMMP9(マトリックスメタロプロテアーゼ9)やシステインプロテアーゼといったタンパク分解酵素によって骨基質が分解される(骨吸収)
破骨細胞のファルネシルピロリン酸合成酵素(Farnesyl Pyrophosphate Synthase, FPPS)は、メバロン酸経路の重要な酵素であり、イソプレノイドの合成に関与します。具体的には、FPPSはファルネシルピロリン酸(FPP)の生成を触媒します。
破骨細胞の骨吸収機能にとってFPPSの活性は重要です。FPPSの阻害は、破骨細胞の機能を抑制し、骨吸収を減少させることが知られています。このメカニズムは、ビスフォスフォネートという骨粗鬆症治療薬の作用機序の一部です。ビスフォスフォネートはFPPSを阻害することで、破骨細胞の活性を低下させ、骨吸収を抑制します。
- 骨髄幹細胞の分化
- 軟骨について
- 骨芽細胞
- 破骨細胞
- 薬物の骨に与える影響
コメントor補足情報orご指摘あればをお願いします。
- << 前のページ
- 次のページ >>


