関連ページ
頻脈性不整脈とは
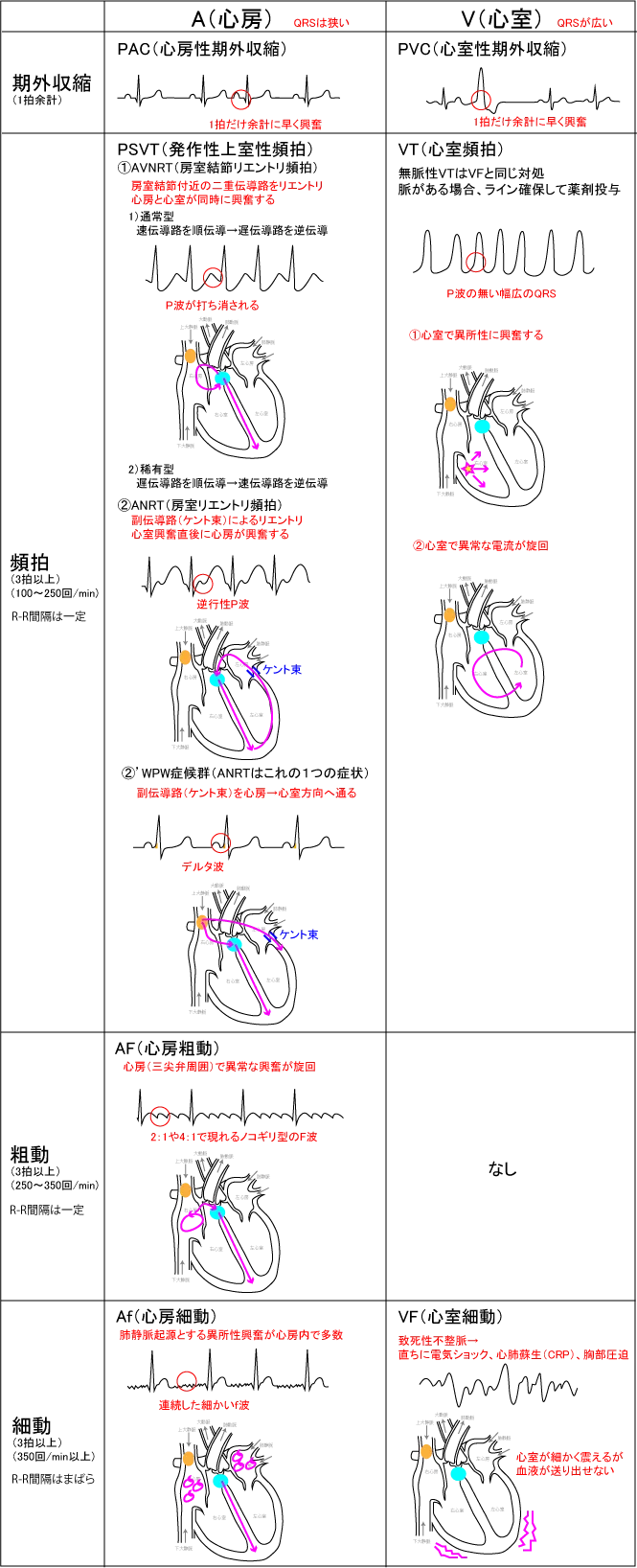
頻脈の種類を知るためにまずはQRS間隔を確認することが重要。QRS間隔が正常でHR↑→心房性(上室性)不整脈、QRS間隔が広くて(小3マス以上)HR↑→心室性不整脈。
- HR≧100回/min (R-Rが大3マス)
- HR≧150回/min (大2マス) →要治療
その異常波が1拍だけなら期外収縮、3拍以上連続していてれば他の不整脈。R-R間隔がまばらで波形がバラバラなら心室細動、f波が見られれば心房細動。R-R一定でP波がなくQRSが広ければ心室頻拍、QRSが狭ければ房室結節リエントリ頻拍、この時P波があるが、逆行性P波なら房室リエントリ頻拍、ワイドQRS、P波上向きでデルタ波があればWPW症候群、心房粗動はAVNRTと見分けがつきにくいが、4:1や2:1ノコギリ波と迷走神経刺激に反応するかどうかで見分ける。
- 期外収縮・・・1拍だけ余計に早く
- 頻拍・・・3拍以上、100~250回/分
- 粗動・・・3拍以上、250~350回/分
- 細動・・・3拍以上、350回/分以上
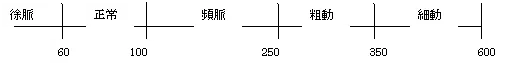
一般に心拍数と呼ばれるものはR-R間隔、心房の興奮回数ではなく、心室の単位時間あたりの興奮回数である。すなわち、心房細動の350回/分以上は心拍ではなく、心房の興奮回数/分ということになる。
期外収縮
予期される収縮より早期に収縮を起こす。基本的には治療の必要はないがQOL低下等、薬物治療をしなければならない状態であれば以下のように行う。
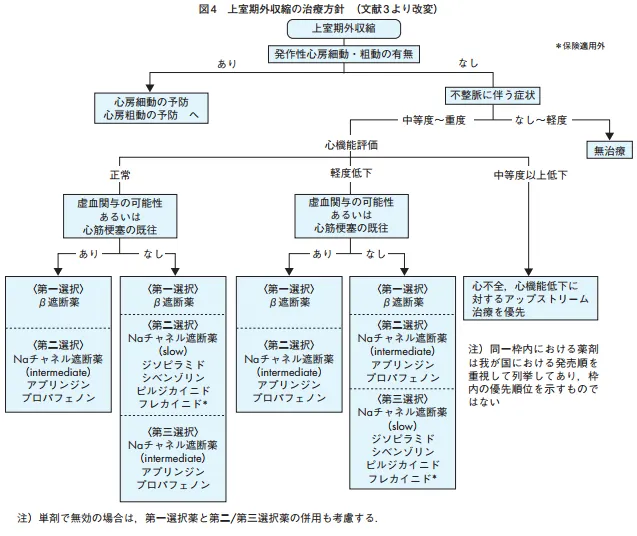
上室性期外収縮(PAC)は心機能が正常or軽度で虚血関与の可能性や心筋梗塞の既往がないならβ遮断薬が第一選択、第二選択はslowのNaチャネル遮断薬。虚血があるなら第一選択がβ遮断薬、第二選択がmedのNaチャネル遮断薬のアスペノンやプロノン。中等度以上の心機能低下はアップストリーム治療
β遮断薬は心房と結節にしか作用せず、房室伝導を抑制し、心房のERPを延長させる効果が期待できる。細胞内のNa+を低下させるNaチャネル遮断薬は、代償的にNa-Ca交換機構にてNa+流入と引き換えにCa2+が流出するので心収縮力が抑制されるため、心機能抑制例には使用しない(使用するとしたらfastのⅠb群)。
期外収縮に限らず、他の不整脈においても正常か器質的心疾患(肥大心,不全心,虚血心)があるかで使用する薬剤が異なっている。肥大心とは心電図上ST変化を伴った左室肥大を、不全心とは左室駆出率40%以下の収縮不全を、虚血心とは梗塞をすでに認めるか虚血が繰り返し出現する病態をいう。
肥大心も虚血心もSTに変化があるものであれば心筋のどこかしらに虚血があり、虚血があればNa-Kポンプ機能の低下により、代償的にNa-Ca交換機構が活性化してCa2+が細胞内へと流入することによりプラトー相が長くなり?活動電位持続時間(APD)が延長する。
一方、不全心筋では細胞内Na+濃度が増加しているが、これは、① Na-K ATPaseを介する細胞外への Na+放出が減少しているか、あるいは②細胞に流入するNa+が増えているかのどちらかに起因する。細胞内a+濃度の上昇はNa-Ca交換機構を介して細胞内Ca2+濃度をより高く維持するように働く。この作用は小胞体内のCa2+を保持し、不全心筋の収縮を維持するように機能する。その結果、不全心筋ではAPDは長くなる。
一般にこのような器質的心疾患例では,心室筋の伝導時間や再分極時間が延長しており,そこに強力な Na チャネル遮断薬が加わると,心室内伝導遅延が強まり(QRS 波幅の増大),心室内リエントリーを招き,ときに正弦波様心室頻拍を誘発する危険がある.また Na チャネル遮断薬の陰性変力作用によって心不全が悪化することもある.一方,K チャネル遮断作用を有する薬剤が加わると,心室の活動電位持続時間(QT 時間)を延長し torsade de pointesを誘発する危険性があり,そのリスクは病的心ではより高まる。
心室性期外収縮(PVC)は生活習慣の改善(睡眠不足や喫煙など)。心室起源は迷走神経刺激は無効、頻発するならカテーテルアブレーション。
上室頻拍
心房頻拍含め幾つか種類があるが、発作性上室性頻拍(PSVT)が90%を占めるため、上室性頻拍=PSVTというイメージが強い。
PSVTはAVNRT(房室結節リエントリ頻拍)とANRT(房室リエントリ頻拍or房室回帰性頻拍)の2種類ある。
AVNRTは房室で異常電流が旋回して、心房と心室が同時に興奮する。そのため心房の興奮が心室に打ち消されてP波が見えなくなる。
AVRTは心室興奮直後に刺激がケント束を通り、心房が興奮する。通常右心房→房室結節へと伝わるところ、左心房側から房室結節へ伝わるので電流が逆向きとなり、逆行性P波を形成することが特徴。
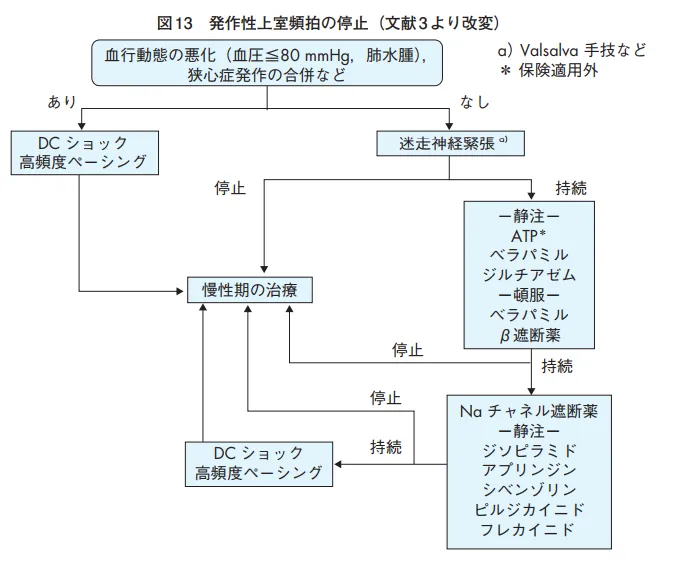
治療としては、房室結節が原因なので、迷走神経刺激によく反応することから、迷走神経刺激→無効ならATP(ATPは分解によりアデノシンへ。でも保険適応外)→無効ならベラパミル、ジルチアゼム→無効ならⅠ群投与。
M2、アデノシン刺激はI(K.Ach)増加で房室結節伝導抑制、I(Ca.L)抑制で房室結節はL型Ca2+チャネル電流なのでリエントリー回路の遮断。
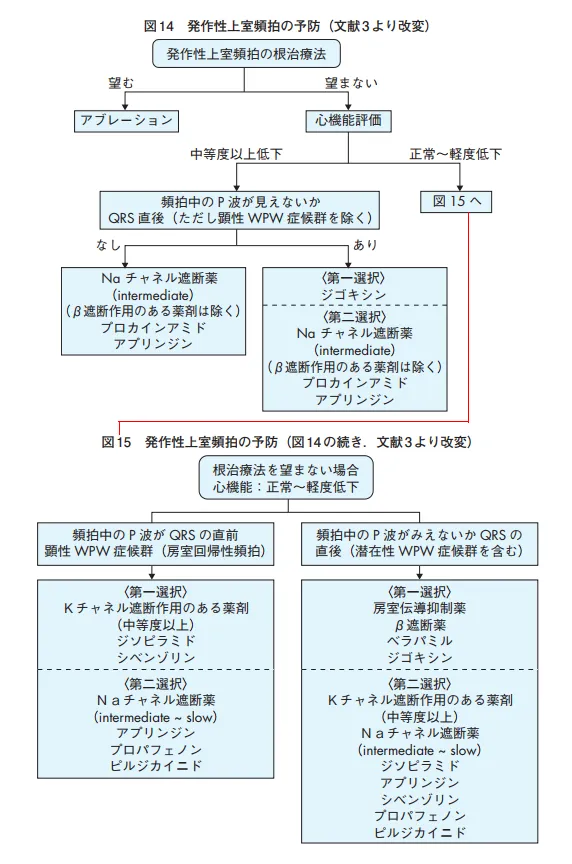
その後の再発予防としては、基本カテーテルアブレーションだが、希望しないor不成功の場合、再発予防治療へ(図14~図15)。
房室結節は副交感神経が高密度支配している。眼球圧迫(Asher法)、息をこらえる(Valsalva法)、深呼吸、顔面浸水等もあるが、眼球圧迫は網膜剥離リスクのため非推奨、Valsalva法が最も効果があり(50%)推奨。
WPW症候群
同じケント束が関与する疾患にWPW症候群があるが、これは心房→心室の順に興奮が伝わる(逆回り)ことからP波は上向きだが、ワイドQRSとデルタ波が見られることが特徴。AVRTはWPW症候群に伴う不整脈である。
注意するべきは潜在性WPW症候群(心電図上明らかなデルタ波無いもの)の房室回帰性頻拍は房室伝導抑制作用を有する薬剤が推奨ですが、顕在性WPW症候群(心電図上デルタ波があるもの)では心拍は正常なのでレートコントロールに使うジゴキシン、ベラパミル、β遮断薬のは使用不可となっていること。
WPW症候群ではまずアブレーション、薬は洞調律維持作用のあるⅠaとⅠc群(主としてプロカインアミド)が使用される。。
心室頻拍
心室頻拍(VT)は、心室で異所性に興奮する(異常自動能)or心室で異常な電流が旋回(リエントリー)を原因として起こり、時間とQRSと虚血性心疾患の有無で更に分類される。
- 時間で分類・・・非持続性VT(30秒以内)、持続性VT(30秒以上)
- QRSで分類・・・単形性VT(単一のQRS波形)、多形性VT(単一ではない)
- 虚血性心疾患の有無・・・特発性(虚血性心疾患を伴わない)
特発性単形性非持続性VTで軽度の場合は、PVCと同様薬物療法が必要ない。
持続性VTで血圧が保たれている場合、不安定な場合DCショック、安定で心機能低下例にはKチャネル遮断薬、Ib群、心機能低下がない例にはNaチャネル遮断薬はⅠaではプロカインアミド、Ⅰb群、Kチャネル遮断が推奨されている。
特発性VTのうち右脚ブロック左軸偏位型(RBBB+LAD)は左脚後枝領域のCa電流依存性組織におけるリエントリーが原因で、ベラパミル等のCa拮抗薬を使用、第二選択はβ遮断薬。左脚ブロック右軸偏位型(LBBB+RAD)は交感神経(カテコラミン)が関与、ATP、β遮断薬(プロノン含む)、Ca拮抗薬、Ⅰ群、カテーテルアブレーション。なお、ベラパミルとATPは適応外。
再発予防は基礎心疾患がなければカテーテルアブレーション、無理なら上記の薬剤、基礎心疾患があるなら植込み型除細動器(ICD)、無理ならKチャネル遮断やβ遮断薬、ベプリコールを使用。心疾患があるのでNaチャネル遮断薬は使用しない。
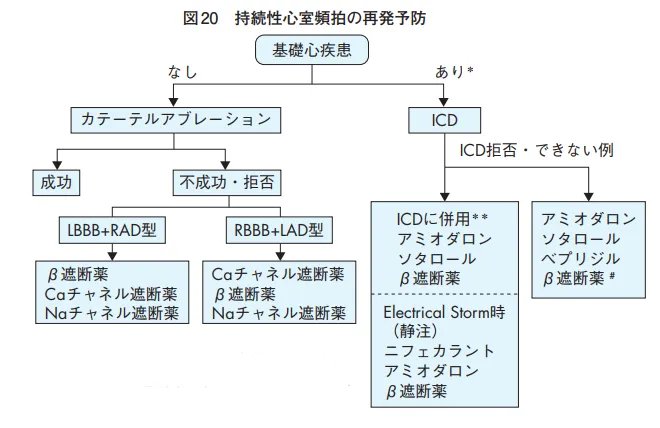
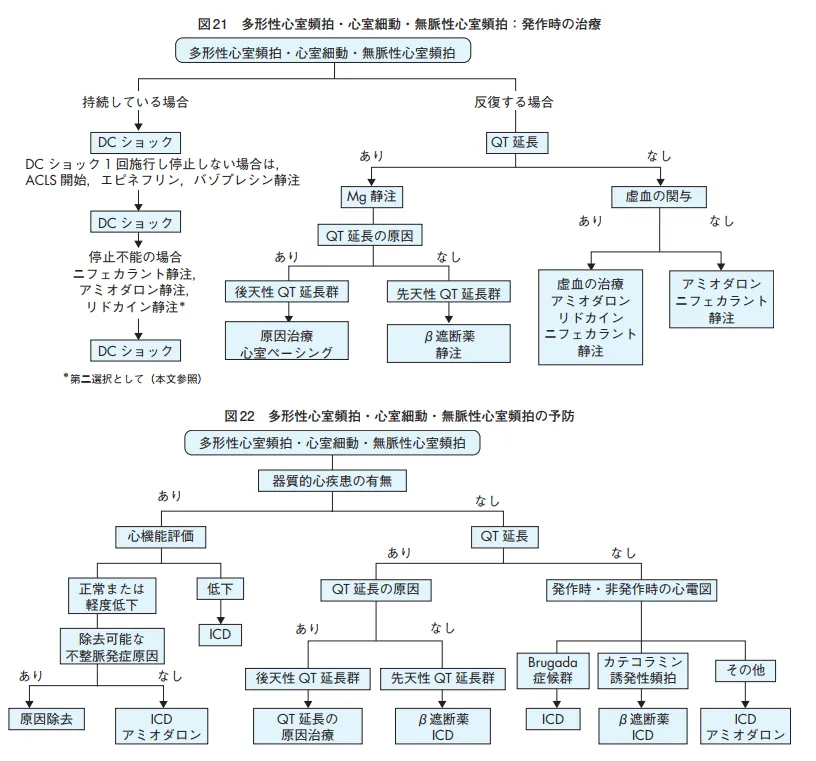
多形性心室頻拍にはQT延長症候群と非QT延長症候群がある。
QT延長症候群(LQT10まであり、LQT1~3で90%)は、心筋細胞膜のイオンチャネルを支配する遺伝子変異による先天性と薬剤による後天性がある。これに含まれる形で心室性期外収縮からのRonTが引き金となって心内膜細胞側のプルキンエ細胞の早期化脱分極からのトリガー活動で起こるトルサドポアンがある。
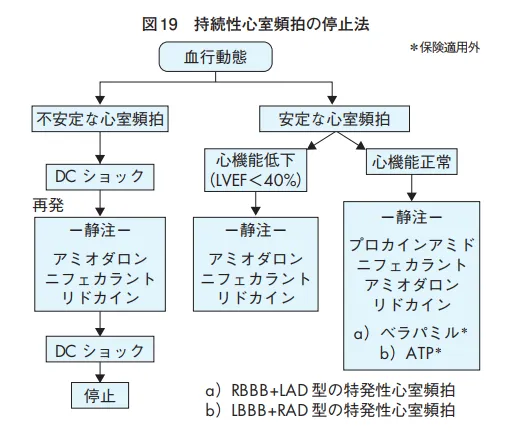
多形性心室頻拍治療は、心房細動と無脈性VTの治療プロトコルと同じで、持続はDCショック、反復する場合でQT延長の場合、硫酸Mgの静注、予防はβ遮断。QT延長がなく虚血の場合は、虚血により心筋収縮力が落ちているため、収縮力低下の少ないリドカインが第一選択。持続性VTやVFへの移行が危惧されるならニフェカラントやアミオダロン。
非QT延長症候群のうち心疾患を伴わずに起こる多形性心室頻拍として、Brugada症候群やカテコラミン誘発性VTがある。前者はICDの適応、後者はβ遮断薬もしくはICDの適応。
基本的に、血行動態(意識、脈拍、血圧、心拍)が保たれている場合、Naチャネル遮断薬、アミオダロン。ニフェカラントはIKrを強力に抑制するがQT延長リスクが大きいため難治例へ。リドカインの停止効果は劣る。血行動態が不安定の場合は電気的除細動。再発予防は、植込み型除細動器、併用でアミオダロン、ソタロールとβ遮断薬。カテーテルアブレーションも有効。
心房粗動
心房粗動(AForAFL)(AFだと心房細動と呼び名がかぶるのでAFLも用いられる)は、心房で異常な電流が右房内三尖弁輪を旋回(リエントリー)。ノコギリのF波を伴う(通常2:1か4:1が多い)。T波は見えない。RRは4マスくらい。
右心房内でリエントリー→下方向へ速い伝導、↑方向へ遅い伝導のため、波形が左右対称ではない。
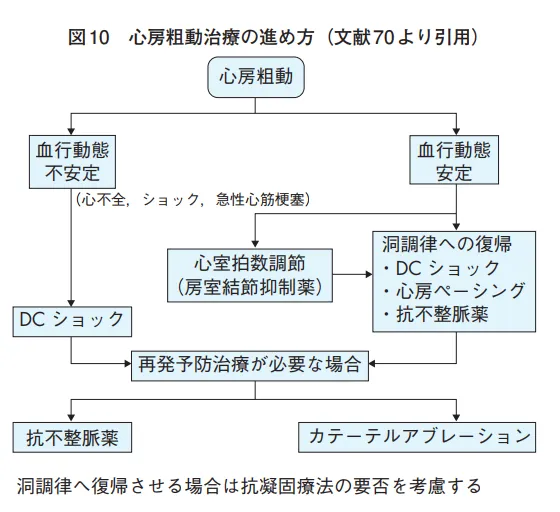
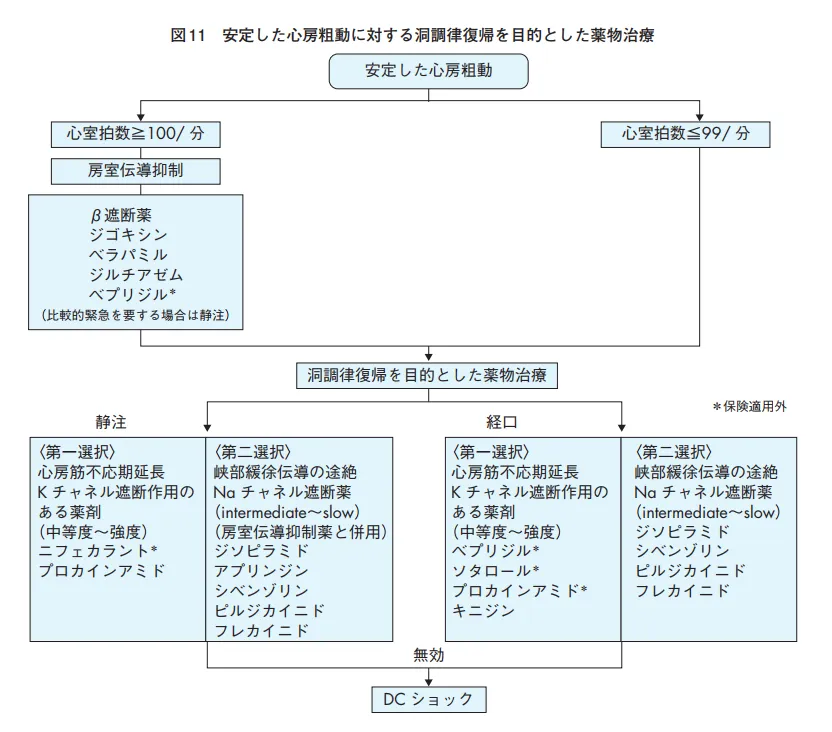
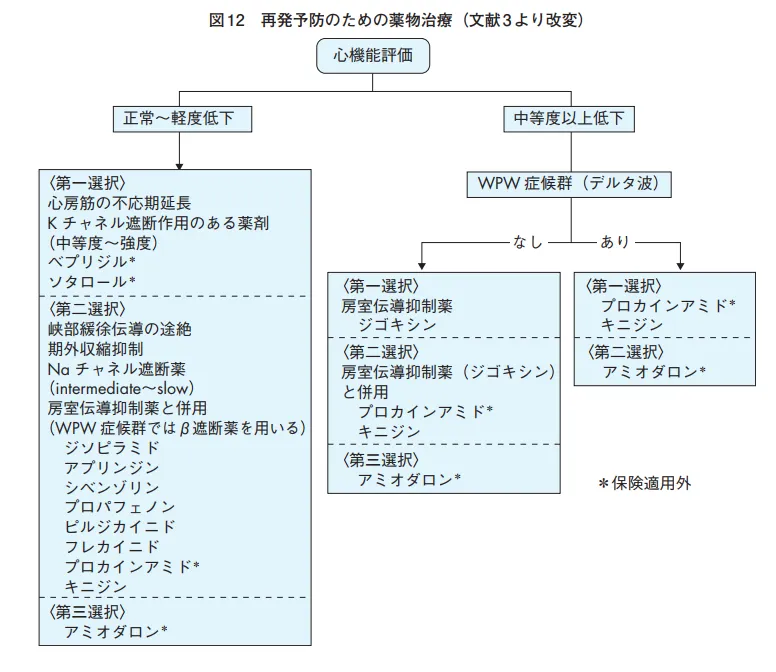
血行動態不安定ならカルディオバージョン→静脈麻酔後、Rに同期50Jで通電。安定なら第一に房室結節のレートコントロール、ついで心房筋の不応期短縮のKチャネル遮断薬、右房下部の緩徐伝導を抑えるNaチャネル遮断薬。Naチャネル遮断薬は効果は薄い上に、M2遮断による心拍上昇に注意する→予防にあらかじめジギタリス等房室結節抑制薬を投与しておく。
再発予防は心機能低下か正常かで異なる。正常なら心房筋の不応期を延長させるKチャネル遮断薬(ベプリコール含む、アミオダロン含まず?)、第二選択が緩徐伝導の途絶を目的としてNaチャネル遮断薬(上記同様房室結節抑制薬併用)、第三選択がアミオダロン。心機能低下でWPW症候群(デルタ波)がなければジゴキシン、併用で心機能抑制作用が比較的弱いプロカインアミドかキニジンが第二選択、WPW症候群があるならジゴキシンとβ遮断薬、Ca拮抗薬は避ける(房室結節伝導を抑制し、副伝導路の伝導速度を速め、心室拍が上昇し不整脈が悪化する可能性がある)が、WPWは基本的にアブレーションが第一選択。
心室粗動
心室には粗動に対応する疾患がない。
心房細動
心房細動(Af)は、心房で3~6個の複数異所性興奮が起こり、心房内に同時に旋回(リエントリー)する頻脈性不整脈である。
心室拍数は発作性Afでは120~150回/min以上。RR間隔は3~4マスと一定ではないが頻脈。心房内の血流速度は低下。房室結節の不応期が長いせいで心室まで全ての興奮は伝わらず。
肺静脈近位部の心外膜側には心房筋が袖状に進入しているが、洞結節細胞やPurkinje線維に類似した細胞が存在することが知られており、これが異所性興奮や伝導異常、リエントリーの発生に関係すると考えられている。
この肺静脈起源の期外収縮が引き金となって心房内に複数興奮波のリエントリーが誘発され、心房細動が生じることもあれば、期外収縮が連発し持続性の高頻度発火が心房内に細動様伝導を生じ、単独または心房内リエントリーと複合して心房細動が生じることもある。
とはいえ、発生機序は単一ではない。トリガーとなる異常興奮、心房筋がリエントリーを成立させるための電気生理学的変化(電気的リモデリング)又は構造変化(構造的リモデリング=不整脈基質)が起因。
- 電気的リモデリング・・・Af自体が高頻度興奮による細胞内Ca2+蓄積と膜Ca電流減少→QT短縮、ERP短縮→波長短縮→複数リエントリーが可能に
- 構造的リモデリング・・・Afが長期に持続すると左房の機械的負荷(僧帽弁狭窄や高血圧)によりギャップ結合の変化などが生じる。心房筋肥大、心房線維化、心房筋のイオンチャネルの変化等を引き起こす。特に線維化は伝導速度を減少させるとともに不均一伝導を生じ、リエントリーを起こしやすくする。(この線維化を抑えるのがARB)
心房細動をきたしやすい疾患には、僧帽弁疾患、心不全、心筋梗塞、高血圧、糖尿病、甲状腺機能亢進症(トリヨードサイロニンによる心房筋のKv1.5遺伝子の発現亢進)等がある。
心房細動では、心房内の血液がよどみ、左房内に血栓ができ、できた血栓が椎骨動脈等へと移動して脳動脈を閉塞させる心原性脳塞栓症の原因疾患である。また、心房細動はトロンボモジュリンやPAI-1などの遺伝子発現→易血栓症を引き起こす。
心房細動は今のところ以下のような感じで分類されて、その分類ごとに治療方法をガイドラインで規定している。
- 孤立性心房細動・・・60歳未満で高血圧含め器質的心疾患(肥大心,不全心,虚血心)が全くない
- 初発心房細動・・・心電図上初めてAfを確認
- 発作性心房細動・・・発症後7日以内に正常洞調律へ
- 持続性心房細動・・・発症後7日を超えて持続
- 長期持続性心房細動・・・持続性が1年以上
- 永続性心房細動・・・電気的、薬学的除細動不能
心房細動の治療法
- 初発心房細動・・・心房細動の予防を安易に行わず再発(50%)が無いか見極める。脳梗塞の危険因子があれば抗凝固療法、心筋梗塞や甲状腺など原因除去できるものは抗不整脈薬は不要
- 発作性心房細動・・・発症初期には薬物療法反応するのでQOL低下例には洞調律維持としてトリガーと基質に対して抗不整脈作用を示すNaチャネル遮断薬(slow)を使用する。
ただし、1年で5.5%は持続性へ移行するため、最近は(洞調律維持<心拍数調節)となっていて、房室伝導抑制作用のあるβ遮断薬、Ca拮抗薬が用いられることもある。
これで不十分の場合or心不全合併例はジギタリスやアミオダロンを使用する。
高血圧、心不全、75歳以上、TIA既往、脳梗塞既往、慢性閉塞疾患が持続性への危険因子なので、これらのアップストリーム治療を行うことが推奨されている。
いずれかを選択した場合でも脳梗塞リスクに応じた抗凝固薬は継続する。
夜間・食後のAfは迷走神経が原因の可能性→M2拮抗薬が効果あり→ジソピラミドのように抗コリン作用を併せ持つ薬が効果あり?
カテーテルアブレーションによる肺静脈隔離術(発作は○、持続は△) - 持続性心房細動・・・薬物による除細動はほとんど不可能。心拍数調節がメイン。洞調律を追求するならベプリコール、アプリンジン、ソタロール、アミオダロン。
電気的除細動により94%で洞調律に復する。→しかしその後の再発率高い。 - 永続性心房細動・・・心拍数調節と抗凝固療法にて維持し、洞調律にはこだわらない。
安静時心拍は60~80回/minとし、130異常にはしない(うっ血性心不全を惹起)
アップストリーム治療として、高血圧には心房の線維化や肥大を抑制するARB、ACE阻害を中心とした降圧を、HMG-CoA阻害薬はコレステロール抑制作用とは全く別に電気的・構造的リモデリングを抑制し,心房細動の誘発性を低下する作用があるので高脂血症合併例では積極的に使用する。
心房細動への一般的な薬剤使用として、CHADS2スコアで1点以上あれば抗凝固療法を行うことがまず第一で、抗凝固療法を行った上で、洞調律<心拍調節の考えに従う。
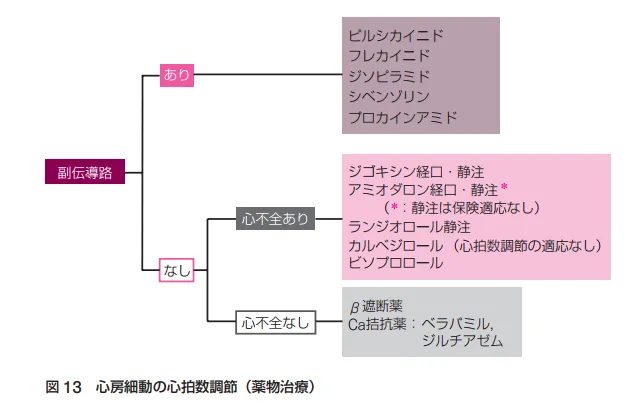
副伝導路(ケント束)があるなら房室伝導抑制作用のあるジゴキシン、β遮断、Ca拮抗薬が使えないのでNaチャネル遮断薬(slow)を使用する。副伝導路がなく心不全合併例には、心室に対する催不整脈作用や陰性変力作用のあるNaチャネル遮断薬が使えないのでジゴキシン、αβ遮断薬、Ca拮抗作用とαβ遮断作用を持つアミオダロンを使用する。心不全がなければβ遮断薬かCa拮抗薬を用いる。
続いて洞調律化(除細動)においては、血行動態(意識、脈拍、血圧、心拍)が不安定もしくは、血行動態が安定でも器質的心疾患(肥大心,不全心,虚血心)があるならカルディオバージョンを行う。
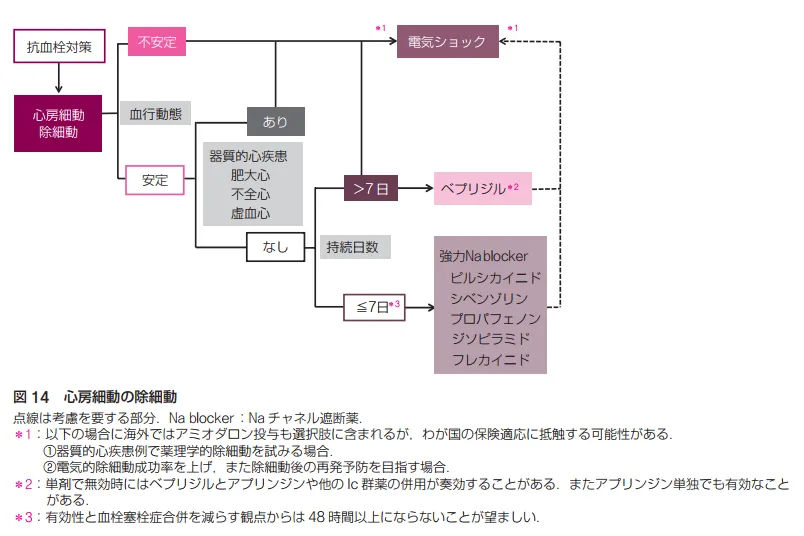
器質的心疾患がなく、発作性であればNaチャネル遮断薬(特に強力なⅠc群:サンリズム、プロノン、タンボコール、もしくはⅠa群:シベノール、リスモダン)、持続性だとNaチャネル遮断の効果は薄いので、Ca拮抗作用とKチャネル遮断作用を併せ持つベプリコールを使用する(アミオダロンやアプリンジンも効果があるとは言われている)。
心房細動の再発予防についても洞調律や心拍調節とほぼ同じようなプロトコルであり、抗凝固療法を前提に、器質的心疾患がればアップストリーム治療をしながら、Kチャネル遮断薬を使用。器質的心疾患がなければNaチャネル遮断薬、薬剤抵抗性の場合はカテーテルアブレーションが考慮される。
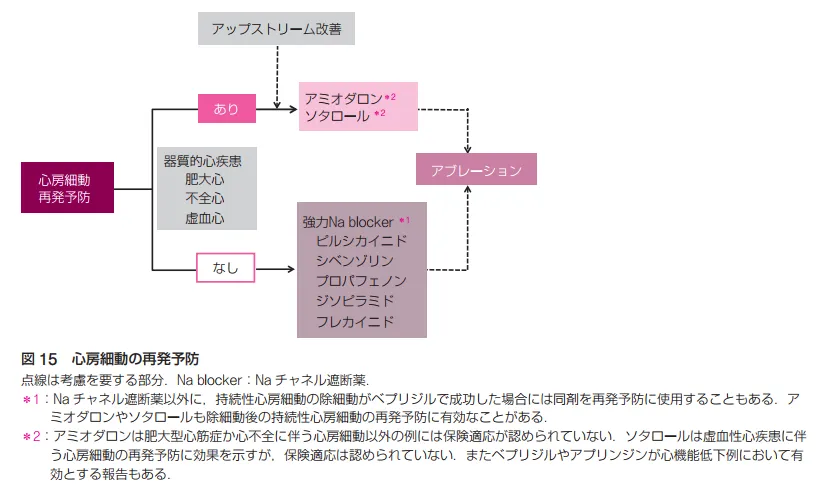
その他、合併症に応じて薬剤を選択する。
狭心症、心筋梗塞は心拍の増加と心拍出量の低下で病態が悪化するのでNaチャネル遮断薬は非推奨、Kチャネル遮断薬を使用。
COPD等呼吸器疾患には、β遮断薬、PDE阻害薬(テオフィリン等)は避ける。Ca拮抗薬の心拍数調節にて対応。
甲状腺にはβ遮断薬による心拍調節。使えないならCa拮抗薬。
WPW症候群はカテーテルアブレーションによる副伝導路の遮断。房室伝導抑制作用のある薬は使わず、薬剤としてはプロカインアミドがよく用いられる。
心室細動
心室細動(VF)は心室が細かく震えるが血液が送り出せない状態で、心電図波形もQRSの広いバラバラの波形となる。
無脈性VTと共に直ちにAEDを始めとしたDC(直電)ショックと心肺蘇生(CPR)が必要。
(参考文献/サイト/図引用元他)
関連ページ
コメントor補足情報orご指摘あればをお願いします。
- << 前のページ
- 次のページ >>


