目次
貧血の検査値
臨床検査値を参照
貧血の診断
鑑別診断には血清鉄や貯蔵鉄だけでなく、MCV(平均赤血球容積:Ht/RBC)やMCHC(平均赤血球Hb濃度:Hb/Ht)、MCH(平均赤血球色素量:Hb/RBC)、Ht(ヘマトクリット:血液中の赤血球が占める割合)を測定し、赤血球の大きさや色素を調べることも必要である。
| 小球性低色素性貧血 | 正球性正色素性貧血 | 大球性貧血 | |
|---|---|---|---|
| MCV | 低(80以下) | 正常(81~100) | 高(101以上) | MCHC | 低(30以下) | 正常(31~35) | 正常(31~35) | 鑑別疾患 | ・鉄欠乏性貧血 ・無トランスフェリン血症 ・鉄芽球性貧血 ・サラセミア ・慢性疾患による貧血 |
・溶血性貧血 ・出血性貧血 ・腎性貧血 ・再生不良性貧血 ・MDS |
・巨赤芽球性貧血 ・再生不良性貧血 ・MDS |
| 疾患名 | 機序 | 検査値など |
|---|---|---|
| 再生不良性貧血 | 幹細胞低下 | Fe↑、フェリチン↑、UIBC↓、EPO↑、血球は正常なのでLDH等は上がらない |
| MDS(骨髄異形成症候群) | 幹細胞異常 | 異形なのでLDH↑、間接型ビリルビン↑、好中球ALP→(CMLは↓) |
| 腎性貧血 | EPO低下 | Hb13未満、EPO↓ |
| 巨赤芽球性貧血 | VB12・葉酸低下 | 異形なのでLDH↑、間接型ビリルビン↑ |
| 鉄欠乏性貧血 | 血清鉄低下 | Fe↓、フェリチン↓ |
| 無トランスフェリン血症 | 血清鉄低下 | Fe↓、フェリチン↑、トランスフェリン↓ |
| 鉄芽球性貧血 | ヘム合成異常 | Fe→or↑、フェリチン↑、LDH↑、間接型ビリルビン↑、TIBC↓、骨髄内(環状鉄芽球↑) |
| サラセミア | グロビン合成異常 | Fe→or↑、フェリチン↓、Hb↓、骨髄内(鉄芽球→or↑)、LDH↑、間接型ビリルビン↑ |
| 溶血性貧血 | 赤血球破壊 | LDH↑、AST↑、間接型ビリルビン↑↑、ハプトグロブリン↓ |
小球性低色素性貧血
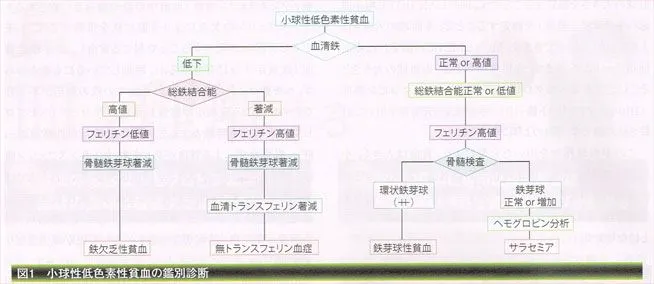
全てヘモグロビンの合成阻害が原因。
鉄欠乏性貧血
小球性低色素性貧血のほとんどが鉄欠乏性貧血であり、鉄欠乏性貧血では血清鉄とフェリチンが低下するが、TIBCは増加する(沢山の鉄を運ぼうとするため)
血清鉄が低いだけでは、鉄欠乏性貧血か無トランスフェリン血症かが判別できないので注意を要する(無トランスフェリン血症では貯蔵鉄:フェリチンが高い)。
鉄欠乏性貧血では貯蔵鉄が回復するまで(Hb≧12、TIBC<360、フェリチン≧12)鉄剤を投与する。
鉄芽球性貧血
鉄芽球性貧血は骨髄におけるヘムの合成阻害が原因で起こる貧血で、異形の環状赤血球が産生されるのが特徴。
環状赤血球は鉄芽球性貧血に特徴的な骨髄内の赤血球前駆細胞です。環状赤血球は、ヘム合成の障害により鉄が異常に細胞内に蓄積した結果生じます。この鉄の蓄積は、細胞のミトコンドリア周囲にリング状に見られることが多いため、この名前が付けられています。
環状赤血球は鉄芽球の一種であり、特に鉄のリング状の沈着が特徴的な赤血球前駆細胞を指します。鉄芽球性貧血の診断においては、特に環状赤血球の存在が重要な指標となります。確定診断には骨髄検査が必要です。
血液検査では、ヘモグロビンの低下、フェリチンと血清鉄は正常または増加、TIBCは低下している。環状赤血球は異形なので脾臓で壊され、LDHと間接型ビリルビンは上昇する。
先天性鉄芽球性貧血は、遺伝子変異によって引き起こされます。これらの変異は、ヘム合成経路の特定の酵素の活性を減少させることが多く、その結果、ヘムの合成が不十分になります。
後天性鉄芽球性貧血は、薬物、アルコール、鉛中毒、または特定のがんなど、さまざまな条件や露出によって引き起こされることがあります。これらの因子は、ヘム合成経路を直接または間接的に阻害することができます。
サラセミア
サラセミアは骨髄におけるグロビンの合成阻害が原因で起こる貧血で、異形の標的赤血球が産生されるのが特徴。
- α-サラセミア: α-グロビン鎖の合成が影響を受けます。人は通常、α-グロビン鎖をコードする遺伝子を4つ持っています(各染色体に2つずつ)。α-サラセミアは、これらの遺伝子の一つ以上が欠損または機能不全である場合に発生します。
- β-サラセミア: β-グロビン鎖の合成が影響を受けます。β-サラセミアは、β-グロビン鎖をコードする遺伝子の変異によって引き起こされます。人はβ-グロビン鎖をコードする遺伝子を2つ持っています(各染色体に1つずつ)。
サラセミアの症状は、一般的には貧血、黄疸、腹部膨満、成長の遅れ、顔面骨の変形などが見られます。
血液検査では、赤血球数は正常又は増加しているのにかかわらずヘモグロビン濃度が低下しています。MCVが低下し、MCHも低下しています。標的赤血球は異形なので脾臓で壊され、LDHと間接型ビリルビンは上昇する。
慢性疾患に伴う貧血
別名慢性疾患性貧血は、慢性感染症、慢性炎症性疾患、自己免疫疾患、および悪性腫瘍などの慢性疾患が原因で発生する貧血の一形態です。
この種の貧血は、鉄の利用障害、鉄のホメオスタシスの変化、およびエリスロポエチン(赤血球を生成するためのホルモン)の産生または反応の低下によって特徴づけられます。
慢性疾患性貧血における鉄の利用障害は、以下のメカニズムにより生じます:
- 炎症性サイトカインの影響: 慢性疾患や炎症に伴い、サイトカイン(特にインターロイキン-6など)のレベルが上昇します。これらのサイトカインは、肝臓でヘプシジンというペプチドホルモンの産生を刺激します。ヘプシジンは腸での鉄の吸収を抑制し、体内の鉄の放出を減少させることにより、血液中および体内の鉄の量を制御します。その活性が高まると小腸からの鉄の吸収が抑制されるため、貧血になる。
- 鉄の利用障害: ヘプシジンの増加により、鉄がマクロファージ(鉄を貯蔵する細胞の一種)内に留まり、骨髄での赤血球の産生に使用される鉄が不足します。これにより、赤血球の産生が減少し、貧血が引き起こされます。
- エリスロポエチンの産生減少: 慢性疾患によって腎臓の損傷が生じると、エリスロポエチンの産生が減少することがあります。エリスロポエチンは赤血球の産生を促進するため、その減少は貧血をさらに悪化させることになります。
慢性疾患性貧血の治療は、根本的な慢性疾患の管理に焦点を当てます。鉄補給療法は一般的には推奨されませんが、ヘプシジンの活性や鉄の代謝に基づいて、特定の状況下では有益である可能性があります。また、重度の貧血に対しては、エリスロポエチンの補充療法が適用されることもあります。
正球性正色素性貧血
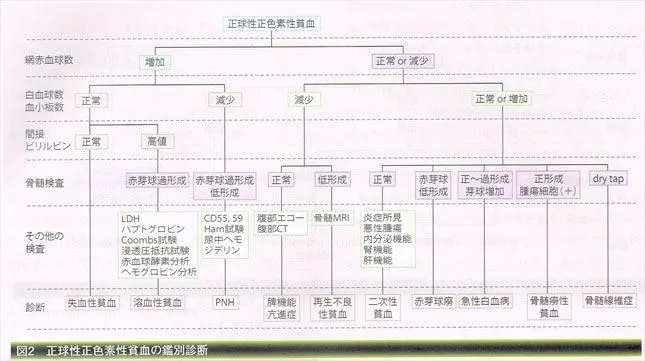
代表的なのは溶血性貧血、再生不良性貧血、腎性貧血。
赤血球を作ることが出来れば網赤血球数(若い赤血球)が増加するので、赤血球を作ることが出来ない再生不良性貧血や腎性貧血では網赤血球数は減少し、作られた後に壊される溶血性貧血では網赤血球数は増加する。
溶血性貧血
網赤血球数が増加していて消化管出血がなければ、溶血性貧血を疑う。
溶血性貧血は骨髄で赤血球が作られるものの、血管内や血管外で作られた赤血球が壊される。細胞が壊されるときに上がる検査値として、LDHやAST、間接ビリルビンが上昇し、ハプトグロブリン(主に赤血球の分解から生じるヘモグロビンを結合し、除去する役割)が低下することが特徴。
血管内溶血
血管内溶血は、血中で補体系の活性化、特定の抗体の存在、および血栓形成により赤血球が破壊されることで引き起こされます。
-
何らかの原因で補体の制御に関するPIGA遺伝子が変異して、補体系による直接的な細胞破壊を受けてしまうことで赤血球が溶血してしまう。PNH(発作性夜間ヘモグロビン尿症)が代表。赤血球以外にも白血球や血小板も低下する。
診断はフローサイトメトリーで赤血球細胞表面にGPIアンカー(CD59、CD55)がないことを確認。治療は補体を阻害するエクリズマブ、ステロイド、補体を除いた洗浄赤血球の輸血。血小板が低下するがなぜか血栓できるので、あればヘパリンやワーファリン等。 - 自己免疫性溶血性貧血(冷式AIHA:アイハ): 体が自分自身の赤血球を異物と認識し、それに対するIgM抗体やDL抗体を生成する疾患。37度未満で反応し自己免疫性溶血性貧血の1割を占める。CADとPCHの2タイプあり共に血管内で赤血球が抗体に壊される。治療は保温。診断はクームス試験(赤血球に対する自己抗体に対する抗体を加えて凝集させる抗体検査:陽性は2型アレルギー)。
- TTP、HUS、DIC、人工心臓弁やその他の血管内デバイスによる赤血球の損傷等で血栓が血流を阻害し、赤血球が物理的に破壊される(機械的溶血)ことがあります。
血管内溶血では、ヘモグロビンの分解産物である鉄を含む顆粒状の物質(ヘモジデリン)が増加し、通常尿中にみられないヘモジデリンが尿中で増えるのが特徴。血管外溶血では尿中ヘモジデリンは陰性である。
血管外溶血
血管外溶血は、産生された赤血球が以下のような形がおかしい状態になって、主に脾臓で破壊されることで引き起こされます。
脾臓は、主に血液の浄化と免疫応答の調整に関与しています。具体的には、古い赤血球を分解し、血液中の細菌や他の異物をろ過する役割を持っています。また、脾臓は白血球を生産し、体内の感染に対する防御メカニズムを強化するのにも寄与します。
- 自己免疫性溶血性貧血(温式AIHA): 体が自分自身の赤血球を異物と認識し、それに対するIgG抗体を生成する疾患。37℃以上で反応し自己免疫性溶血性貧血の9割を占める。赤血球に結合した後、移動し脾臓で処理される。治療はステロイド、免疫抑制薬、脾臓摘出。
- 遺伝性球状赤血球症(HS): 常染色体優性遺伝(片方の親の変異遺伝子が伝わればかかる:確率50%)で、赤血球の膜が異常であるために、脾臓で容易に破壊される疾患。小児で見られ、間接ビリルビン増加によるビリルビン胆石が見られること特徴。検査は赤血球浸透圧脆弱性試験。パルボウイルスに感染すると赤血球寿命が下がってさらに症状が悪化するため、かからないように注意する。脾臓摘出が一つの治療法。
- サラセミア: ヘモグロビンの生産に関わる遺伝子の異常により、異常なヘモグロビンが生成され、赤血球が不正常な形状になる病気。
- 鎌状赤血球病: ヘモグロビンの遺伝的変異により、酸素が少ない状態で赤血球が鎌の形をした不正常な形状になりやすい疾患。
- ピルビン酸キナーゼ(PK)欠損症: 赤血球内でピルビン酸キナーゼという酵素が不足していることにより、エネルギー産生が障害され、赤血球が容易に破壊される疾患。
再生不良性貧血と赤芽球癆
再生不良性貧血には造血幹細胞の減少により引き起こされる貧血で、先天性と後天性に分類できます。
先天性の再生不良性貧血にはファンコニ貧血があり、自己免疫疾患や環境因子による後天性再生不良性貧血とは異なり、常染色体劣性遺伝(両方の親から変異遺伝子が伝わるとかかる:確率25%)によって引き起こされます。ファンコニ貧血の患者は、生まれつきの骨髄不全とともに、多くの場合、身体的な異常や発達の遅れを伴います。また、がん、特に血液がん(例:急性骨髄性白血病)や固形腫瘍のリスクが通常よりも高くなります。
後天性の再生不良性貧血には特発性(原因不明で免疫抑制or幹細胞異常が起因)と、二次性(薬剤性等)に分けることが出来る。
共に、全ての汎血球(赤血球、白血球、血小板)が減少(Hb10未満、好中球1500未満、血小板10万未満のうちいずれか2つを満たすこと)しており、鉄が使われないので血清鉄とフェリチン、Epoは上昇、UIBCは低下。
治療法は、
- 免疫抑制薬・・・シクロスポリンなど
- 抗胸腺グロブリン(ATG)・・・ATGは、患者の免疫システム内の特定の細胞を標的とし、骨髄に対する自己免疫攻撃を減少させることが目的です。ATG治療は、しばしばシクロスポリンと組み合わせて行われます。
- TPO(血小板生成促進因子)受容体作動薬・・・エルトロンボパグ(血小板生成を促進する薬剤)など、特に血小板数が低い患者に対して有効な治療選択肢です。
- 造血幹細胞移植(Hb7未満、好中球500未満、血小板2万未満が目安)
赤芽球癆は赤血球の産生障害のみが起こっている状態のことで、先天性と後天性の2タイプに分けられます。先天性は生まれつきの遺伝条件によって引き起こされ、最もよく知られているのはダイアモンド・ブラックファン貧血(Diamond-Blackfan Anemia, DBA)で、以下の特徴を持ちます。
- 赤血球の産生が障害される一方で、白血球や血小板の産生には影響がない。
- 遺伝的変異が関与しており、特定のリボソームタンパク質の遺伝子に変異が見られることが多い。
- 治療にはステロイド薬、血液輸血、場合によっては骨髄移植が含まれる。
- 患者は身体的特徴(例:短指症)、成長遅延などの先天的異常を持つことがある。
後天性赤芽球癆は、生涯のどこかで発症し、多くの場合、他の疾患や条件、薬剤の影響、自己免疫反応によって引き起こされます。後天性PRCAの特徴は以下の通りです。
- 特定の薬剤(例:エリスロポエチン製剤)、感染症(例:パルボウイルスB19)、または慢性リンパ性白血病(CLL)などの血液疾患と関連がある。
- 自己免疫疾患の一環として発症することもある。
- 治療は原因を取り除くことに焦点を当てる(例:薬剤の中止、感染症の治療)。
- 免疫抑制療法(例:シクロスポリン、抗胸腺細胞グロブリン)が有効である場合がある。
腎性貧血
腎臓の機能(GFR)が弱り、貧血なのにエリスロポエチンが追加で作られず、EPO分泌が増えない貧血が腎性貧血。これにはエリスロポエチン製剤やHIF-PH阻害剤を使う。
CKDや心不全で炎症性サイトカインが引き起こす慢性炎症では、ヘプシジンの分泌が増加し、さらに血清鉄が低下する。腎血流の低下はRAS活性亢進からのEPO産生反応性低下も拍車をかける。
大球性貧血
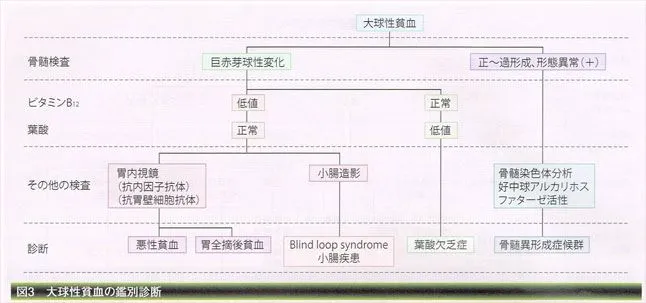
MCV(赤血球の大きさ)が高値。
ビタミンB12や葉酸の不足により赤血球DNAの合成がうまくできず細胞質だけ大きくなった巨赤芽球性貧血がその代表で、症状は鉄欠乏性貧血の症状(疲労感、息切れなど)に加えて、以下の症状が出ることがあります。
- ハンター舌炎・・・舌の表面が異常に滑らかになり、炎症を伴う状態を指します。この状態はビタミンB12欠乏に関連しており、巨赤芽球性貧血の症状の一つとして現れることがあります。舌炎は痛み、燃えるような感覚、味覚の変化を引き起こす可能性があります。
- 亜急性脊髄連合変性症は・・・ビタミンB12欠乏が原因で起こる神経系の障害です。この状態は脊髄の後索と側索が影響を受け、歩行障害、手足のしびれや弱さ、平衡感覚の喪失などを引き起こす可能性があります。重度のビタミンB12欠乏では、これらの神経学的症状が進行し、治療が遅れると不可逆的な損傷を引き起こすことがあります。
巨赤芽球性貧血と悪性貧血
胃が切除されていると胃の壁細胞で作られる内因子分泌が低下してビタミンB12の吸収ができなくなる(胃切除後5年~)。
こうした吸収障害と単なる摂取不足が起因となりビタミンB12が低下する。
また、自己免疫性の萎縮性胃炎によっても胃の壁細胞からの内因子の産生が低下し、これが原因でVB12不足になって引き起こされる巨赤芽球性貧血を悪性貧血と呼ぶ。
悪性貧血では、抗壁細胞抗体と抗内因子抗体といった自己抗体が診断マーカーとなります。また、胃酸の分泌が減少することにより反射的にガストリンの分泌が増えるため高ガストリン血症となります。治療はビタミンB12の補充。
アルコールは葉酸の吸収を阻害したり、葉酸の排泄を増価させたり、代謝で生成するアセトアルデヒドが葉酸代謝に必要な酵素の活動を阻害したりするため、葉酸の欠乏を引き起こす。
妊娠も葉酸の必要量が増えるため、葉酸の不足を引き起こし巨赤芽球性貧血の要因となる。
治療は葉酸の補充だが、葉酸だけ補充するとビタミンB12も鉄を作るときに同時に消費され少なくなるので、VB12も一緒に摂ることが望ましい。
MDS(骨髄異形成症候群)
MDSは骨髄細胞の異常な増殖と成熟の障害によって特徴づけられる一群の異質な疾患で、不効率な血液細胞の生成(不効率造血)を引き起こします。この不効率な血球生成は、異形成赤血球(形態が異常な赤血球)の産生につながり、しばしば大球性貧血を引き起こします。
関連ページ
コメントor補足情報orご指摘あればをお願いします。
- << 前のページ
- 次のページ >>


